last update 2009.04.12
本研究は名古屋大学学部卒業研究、修士研究、博士研究で取り組んだテーマである。現在研究テーマの一部をXAFSを用いた微量元素の局所構造解析に関する研究へ移行している。博士論文の内容は、独立した6編の論文として、学会誌に掲載済みである。また、月刊海洋「現代海洋化学・II」にこの研究の日本語の解説が掲載されているので、興味のある方は参照されたい(太田充恒 (2001) マンガン団塊の希土類元素, 231-238.)。
深海底マンガン団塊は、3d遷移金属元素や希土類元素に富み、1970-80年代にかけて、貴重な海洋資源として注目を浴び、様々な研究が行われてきた。これまでの研究結果より、マンガン団塊は組織、鉱物組成、化学組成などから大きく3種類に分類されてきた。その成因については、種類別に様々な成因が提案されてきたが、不明な点も多く今日に至っている。しかし、本研究では、太平洋及び南極海で採集されたマンガン団塊の化学組成、特に希土類元素存在度パターンとCe異常とCo/(Ni+Cu)比の間に見られる相関関係に注目する事によって、これまで考えられてきた成因的理解を一新する手掛りを得た。
C1コンドライトによって規格化されたマンガン団塊の希土類元素存在度パターンは(下左図)、海洋の化学的堆積物であるにも関わらず、石灰岩などの海洋堆積物や海水よりもむしろ、大陸頁岩のパターンに類似している(下右図)。しかし、そのY/Ho比はコンドライトや平均頁岩よりも小さい値を示し、海水や石灰岩がコンドライトや平均頁岩よりも大きなY/Ho比を持つこととは対照的である。YはHoと類似したイオン半径をもち、価数も同じ3価ではあるが、Yはランタノイドとは異なり Xe core も4f電子も持たない。YのHoからの分別は、イオン半径だけで議論すべきではないことを明らかにした。
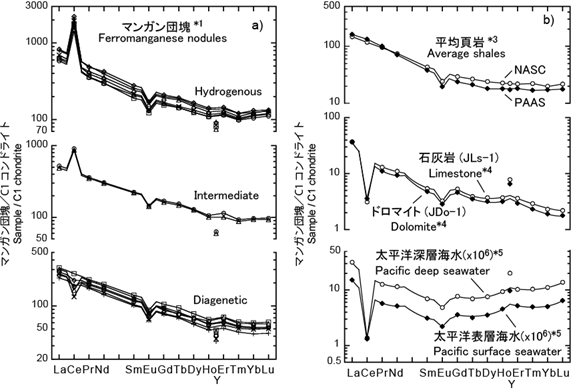
図の説明:データは Ohta et al., 1999 Geochem. J. 33, 399-417., 太田, 2001 「現代海洋化学・II」、231-238 より引用.
Ce異常がMn/Fe, Co/Ni, Co/Cu, Co/Znなどの比と良い相関関係を示すことはすでに知られていたが、今回の研究より、ほぼすべての種類の太平洋マンガン団塊が、Ce異常とCo/(Ni+Cu)の間に強い相関関係を示し、かつ一つの直線上に並ぶことを初めて確認した(下図)。また、非常に酸化的な深層水から形成されたと考えられる南極海マンガン団塊はどの種類の太平洋マンガン団塊よりも高いCe異常値とCo/(Ni+Cu)比を示すことも明らかとなった。Ce異常もCo/(Ni+Cu)比も共に生成時の酸化還元状態を示す地球化学的なパラメーターであると同時に、この元素濃度比はnutrient-型元素に対するscavenged-型元素の濃度比として共通の意味を持つ。その両者に系統的な関係が見られることは、マンガン団塊には種類を問わず、共通した起源物質が存在することを示している。
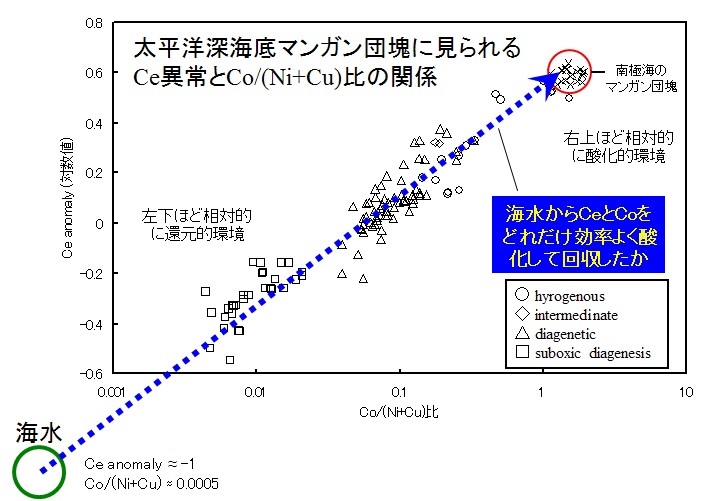
図の説明:データは Ohta et al., 1999Geochem. J. 33, 399-417.; Ohta et al., 1999. J. Earth Planet. Sci. Nagoya Univ. 46, 1-13.より引用.
共通した起源物質として生物起源の粒子が考えられ、次のようなモデル(かなり粗いモデル)を提案した。生物生産の不活発な地域では生物起源粒子が海底に達する前に分解されるため、粒子を覆っていた鉄-マンガン水酸化物はコロイド物質として海水中に取り残される。また、有機物供給量が少ないため、海底は酸化的な環境となる。沈降速度が遅いコロイド物質は十分にCeやCoを取り込みながらゆっくり海底面へ向かって沈降し、最後にCe異常、Co/(Ni+Cu)比共に高い値を取るマンガン団塊を形成する。一方、生物生産の活発な地域では大量の生物起源粒子が分解を免れて海底に供給される。そのため、海底は多量の有機物を分解するために、酸素が多く使用され、比較的還元的な環境となる。生物起源粒子はコロイド物質に比べ沈降速度が速く、粒子を覆っている鉄-マンガン水酸化物はCeやCoを十分に取り込む前に海底に達するため、低いCe異常とCo/(Ni+Cu)比を持つマンガン団塊を形成されると考えられた。
マンガン団塊を含む鉄-マンガン堆積物は希土類元素を高濃度に含有しており、海水との間の分配反応は重要な地球化学的反応である。海洋におけるその分配反応に対しては、希土類元素と炭酸イオンとの錯体生成が大きな影響を与えることが予想される。そこでまず水酸化鉄(III)とNaCl水溶液間(疑似マンガン団塊と疑似海水間)の希土類元素の分配実験を行い、分配係数が水溶液中の炭酸イオン濃度の増加に伴いどのような変化を示すかを調べると同時に、炭酸錯体生成定数をも求めることを試みた。
水酸化鉄(III)とNaCl水溶液間の希土類元素の分配係数のパターンには、水溶液中の炭酸イオン濃度に関わらず、小さい正のCe異常、YのHoに対する分別、上に凸のテトラド効果といった共通の特徴が見られた。しかし、水溶液中の炭酸イオン濃度が増加するに従って、軽希土類元素側の分配係数が重希土類元素側に比べ相対的に大きくなる、YのHoに対する分別が小さくなる、テトラド曲線の膨らみが小さくなるなどの傾向が見られた。用いた実験系の中では炭酸イオン濃度が10−4.80–10−4.59 mol/lの時の系がもっともよく天然系の分配係数の特徴を再現しており、この炭酸イオン濃度は海水の値(10−4.67–10−4.30 mol/l)とよく一致する。この実験結果より、海水で起きている希土類元素の分別には炭酸イオン(希土類元素-炭酸錯体)が非常に重要な役割を果たしていることが分かる。しかし、残念ながら、この実験系では大きな正のCe異常は再現することができなかった。後述するが、これは鉄水酸化物とともにマンガン団塊・クラストの重要な構成鉱物であるδ-MnO2(二酸化マンガンの鉱物)によって引き起こされることが分かっている。
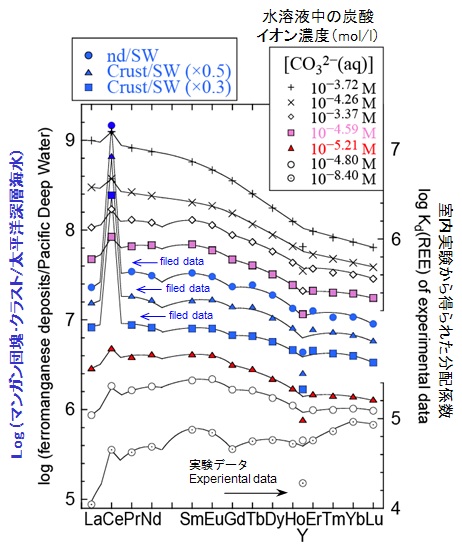
図の説明:nd, NCP, SCP, SWはそれぞれ、太平洋深海底マンガン団塊, 北及び南太平洋マンガンクラスト, 太平洋深層海水を表す。データはBau et al., 1996, Geochim. Cosmochim. Acta 60, 1709-1725; Kawabe et al., 1998, Geochem. J., 32, 213-229.; Ohta et al., 1999. Geochem. J., 33, 399-417; Ohta and Kawabe., 2000, Geochem. J., 34, 439-454. より引用。青色のポイントは、マンガン団塊・クラスト中の希土類元素濃度を海水のそれで割った値(海洋で起きている見かけの希土類元素分配係数)を表す。天然系の見かけの分配係数パターンを再現すべく、室内再現実験を行い、そこで得られた値(Kd = 鉄水酸化物中の希土類元素濃度/水溶液に残った希土類元素濃度)と比較した(室内実験のデータはOhta and Kawabe, 2000. Geochem. J., 34, 455-473 より引用)。ただし、図ではパターンを比較しやすいようにわざと縦軸をずらしている。
また、様々な濃度の炭酸イオンを含む水溶液下で得られた分配係数の結果を用いて、希土類元素(III)-炭酸錯体生成定数を求めることができた。
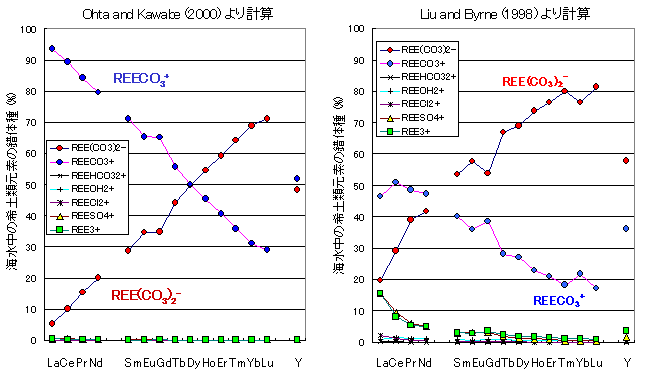
図の説明:海水中の希土類元素の錯体種。炭酸錯体以外は事実上無視できることが分かる。データは Mironov et al., 1982 Koord. Khim. 8, 636-638, Millero, 1992 GCA 56, 3123-3132, Byrne and Lee, 1993 Mar. Chem. 44, 121-130, Liu and Byrne, 1998 J. Sol. Chem. 27, 803-815, Ohta and Kawabe, 2000 Geochem. J., 34, 439-454.から引用。海水のイオン強度はI=0.723で計算
我々の実験結果より得られた錯生成定数は、従来の溶媒抽出法によって得られた値と比べやや大きかった。しかし、重希土類元素ほど大きな値を持つ、上に凸のテトラド効果を示すなど、両者に共通した特徴が多く見られ、溶媒抽出法とは異なる手法でも錯生成定数を求めることが可能であることが分かった。得られた炭酸錯体生成定数を用いて海水中における希土類元素の溶存種を計算した結果、REECO3+(aq)が主要溶存種となり、REE(CO3)2−(aq)が主要溶存種であるというこれまでの報告と異なる。そこで、マンガンノジュールと海水間の希土類元素の見かけの分配係数と室内実験で得られた分配係数を統一的に説明するためには、どちらの錯体が主要溶存種であるべきかを調べた。その結果、REECO3+(aq) が主要溶存種であると考えた方が、実験系と天然系の分配係数の特徴をより統一的に説明できることが判明した。
次に、実験系及び天然系の分配係数と炭酸錯体生成定数に見られるテトラド効果に対し、Refined spin-pairing energy theoryによる解析を行った。テトラド効果の極性と湾曲の大きさは、反応物と生成物における希土類元素イオンのわずかなラカー係数(4f電子の電子反発係数)の差に関係する。炭酸イオンを含まない実験系の分配係数は、上に凸の相対的に湾曲の大きなテトラド曲線を与える。これはREE3+(aq)に比べ、水酸化鉄(III)と共に沈殿している生成物の希土類元素イオン(REE(OH)3·nH2O(ss))の方が相対的に小さなラカー係数を持つためである。希土類元素(III)炭酸錯体生成定数に見られるテトラド効果は、REE3+(aq)よりも炭酸錯体の方がやや小さなラカー係数を持つために生じる。つまり、REE3+(aq)、REECO3+(aq)、REE(CO3)2−(aq)、REE(OH)3·nH2O(ss)の順に、ラカー係数が小さくなることが分かる。炭酸イオン濃度が増加するに従って、テトラド曲線の湾曲が小さくなる理由は、水溶液中でREE3+(aq)に比べ、ラカー係数のより小さな化学種である希土類元素の炭酸錯体の割合が増加するからである。
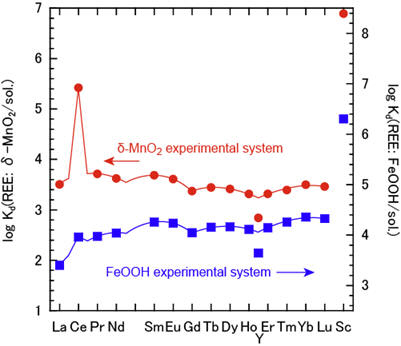
図の説明:データは、Ohta and Kawabe., 2000, Geochim. Cosmochim. Acta, 65, 695-703.より引用。
マンガンノジュールと海水間の見かけの分配係数に見られる非常に大きな正のCe異常は水酸化鉄(III)と水溶液間の希土類元素の分配実験では再現できなかった。大きな正のCe異常の成因としては、鉄-マンガン堆積物の主要構成鉱物の一つであるδ-MnO2が深く関わっていると考えられる。そこで、δ-MnO2と水溶液間の希土類元素の吸着実験を行い、大きな正のCe異常の生成機構を明らかにすると同時に、その分配係数の特徴を調べた。δ-MnO2と炭酸イオンを含まない水溶液間の希土類元素の分配係数には水酸化鉄(III)系の実験結果とは異なり、非常に大きな正のCe異常が確認された。様々な濃度のCe(III)を含む水溶液から、Ceを吸着させたδ-MnO2中のMnの見かけの価数を調べてみると、水溶液中のCe(III)は溶存酸素ではなくδ-MnO2により酸化されることが明らかになった。
希土類元素って?: 研究紹介の補足