last update 2018.10.02
地球化学図は基本的に全濃度、すなわち堆積物中の元素の濃度が「高い・低い」の情報しか示さない。堆積物の表面に吸着した状態なのか、それとも鉱物中に閉じ込められているのかによって、元素の有害性の評価は異なるはずである。また、元素は価数や化学種が異なると毒性や化学・物理的挙動が異なる。たとえばクロムは、三価クロムよりも六価クロムの方が毒性が強くかつ水への溶解度が高い。水銀は、無機水銀よりも有機水銀の方が毒性が高い。そのため、有害元素が環境や生物に与える影響を正しく評価するためには、試料中の全量分析だけでなく、化学形態別に起源や成り立ちを考慮する必要がある。元素形態別地球化学図の作成はこれまであまり例がない。日本の地球化学図では 0.1 mol/l 塩酸を用いた簡易的な形態分析図を提供しているが、どのような元素形態を抽出しているのか分からない。そこで、全国元素形態別地球化学図の作成を目指し、主に以下の3つの項目について研究を進めている。
化学形態別分析法である逐次溶解法には様々な方法が提案されているが、いずれの方法も化学薬品を用いて様々な化学形態で存在する元素の抽出を行っている。今回は、国際的に標準化された手法であるCommunity Bureau of Reference (BCR) 法を用いて、堆積物中の元素存在形態別分析を行う(Ure et al., 1993. Int. J. Environ. Anal. Chem., 51, 135–; Thomas et al., 1994. Anal. Chim. Acta., 286, 423–; Rauret et al., 1999. J. Environ. Monit., 1, 57– )。この方法は、どの実験室で行っても同じ結果が得られるよう手法が統一がされた分析手法である。細かく化学形態を分類することはできないが、繰り返し再現性が高い最も標準的な手法であり、分析の信頼性を評価する標準物質(BCR-701: 湖堆積物)も提供されている(Sutherland, 2010. Anal. Chim. Acta., 680, 10–.)。しかし、標準物質が一つしかない、試料が湖堆積物のみである、認証値がCr, Cu, Ni, Zn, Cd, Pb の6元素と限られているなど、幅広い分野での利活用の点からいくつかの改善が必要である。そこで、地質調査総合センターで提供している地球化学標準物質として提供されている堆積物シリーズ8試料について38元素の存在形態別推奨値を求めた。
| Stage | 試薬 Regent(s) |
反応時間 Reaction time and t |
画分 Fraction |
対象(目的)物質 Target phase(s) |
| Step 1 | CH3COOH (0.11 mol l-1) | 16 hr at 23–25 °C | 酸可溶態 Acid soluble |
イオン交換態・炭酸塩 Exchangeable phase and carbonate |
| Step 2 | NH2OH HCl (0.5 mol l-1, pH 1.5) | 16 hr at 23–25 °C | 還元態 Reducible |
鉄水酸化物・マンガン酸化物 Fe hydroxide and Mn oxide |
| Step 3 | H2O2 (8.8 mol l-1) (repeated twice) | 1 hr at 20–30 °C; 1 hr at 85 °C; evaporation | 酸化態 Oxidisable |
硫化物・有機物 Metal sulfide and organic matter |
| CH3COONH4 (1 mol l-1, pH 2) | 16 hr at 23–25 °C | |||
| Step 4 | HF, HNO3, and HClO4 | 3 hr at 120 °C and then 180 °C for evaporation | 残渣態 Residual |
鉱物 Crystal phase of minerals |
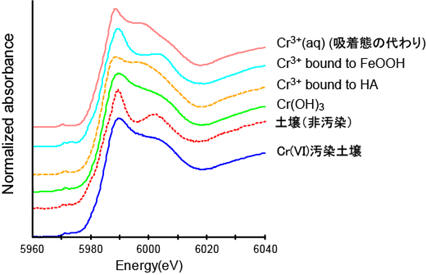
クロムは天然においては難溶性で毒性の低い三価クロムとして存在しているが、六価クロムは非常に水に溶けやすく毒性が高い。六価クロムは環境中で二価鉄・有機物などと反応し時間と共に三価クロムに還元される。つまり、時間と共に六価クロム汚染の痕跡が消えてしまう(高濃度異常が見つかっても、六価クロムそのものが検出されない)。そこで、主にX線吸収微細構造(XAFS)解析法や赤外分光法を用いて、失われた六価クロム汚染の痕跡解明を目指して研究を進めている。
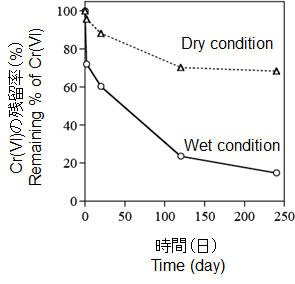
乾燥状態と湿潤状態で土壌中の六価クロムの還元反応を調べた結果、反応がほとんど進まないと考えられた乾燥状態にあっても、六価クロムの還元反応が進むことが明らかとなった(Tsuno et al., 2006. Geostand. Geoanalyt. Res. 30, 55–)。また、一度三価クロムに還元された土壌試料中のクロムは極めて安定な存在形態を持つが、自然由来の鉱物中のクロムとは全く異なる化学形態を持つことが明らかとなった。
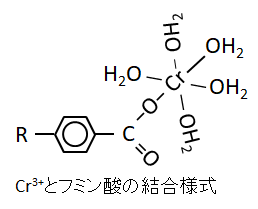
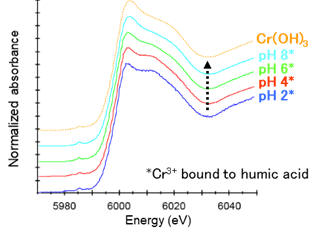
土壌中の主要な還元媒体であるフミン酸と六価クロムが反応した後のクロムの化学形態を、赤外分光法で腐植物質の官能基の視点から、XAFS法でクロムの視点から明らかにした。その結果、六価クロムから三価クロムに還元された後、主にフミン酸中のカルボキシル基と結合することが明らかとなった。また、反応溶液中のpHが高い場合、一部のクロムが(腐植物質と結合せずに)水酸化クロムとして沈殿物を形成することも明らかとなった(Ohta et al., 2011. Bull. Geol. Surv. Japan., 62, 347–; Ohta et al., 2012. Geochem. J., 46, 409–)。
元素の存在形態別分析法は大きく分けて化学形態分析法と物理形態分析法がある。化学的手法は、試薬を用いて目的物質を段階的に抽出する破壊分析法である。元素形態を細かく分割することができる一方、対象外物質の分解や対象物質の抽出が不十分であるなど目的としている化学形態を正しく分析しているのか曖昧な点がある。一方、X線吸収微細構造解析(XAFS)法に代表される物理形態分析法は、非破壊分析法であり、元素の形態情報を比較的正しく捉えることが可能である。しかし、感度が高くないこと(微量元素の分析は難しい)、多数の元素形態が存在する場合、それぞれを細かく区別・認識することが難しいなどの問題点がある。そこで、2つの方法を併用して互いの問題点を補い合うことで、より精度・確度の高い形態分析を目指す。
| 分析法 | 特徴 | 検出限界 | 分類(区分)数 | 形態情報精度 |
| 分別溶解法 | 破壊分析 | 数10 μg/kg | 多成分(3-6)可 | かなり曖昧 |
| XAFS法 | 非破壊分析 | 数10 mg/kg | 2-3成分 | 比較的高い |
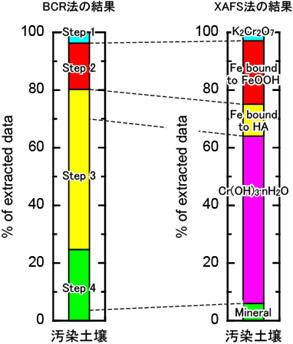
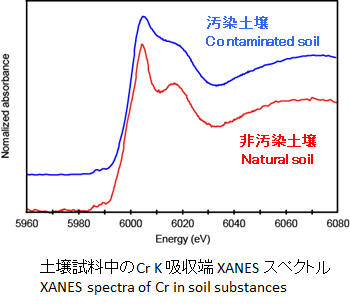
地球化学標準物質において、人為的に六価クロムを添加した土壌試料、人為汚染の影響を受けた都市域河川堆積物(JSd-4)と東京湾堆積物(JMs-1)中のクロムの存在形態を、BCR法とX線吸収端微細構造(XANES)法を併用して明らかにした。汚染のない堆積物試料は、BCR法のどのフラクションでもクロムはほとんど抽出されず、かつXANESスペクトルは互いに類似していた。一方、六価クロムと反応した試料は、step 2(鉄・マンガン酸化物態)と step 3(硫化物・有機物態)のフラクションで多くのクロムが抽出されたが、六価クロムは検出されなかった(人為的に六価クロムを添加した土壌試料のみわずかに残存)。XANESスペクトルで詳細な検討を行った結果、step 3(硫化物・有機物態)と step 4(鉱物)中のクロムのほとんどは水酸化クロムとして存在していることが明らかとなった。故に、六価クロムが環境中で還元反応を受けた場合、一部は水酸化クロムを形成し、一部は鉄水酸化物およびフミン酸と結合する事が明らかとなった(それぞれの比率は試料によって異なる)。
よって、もしBCR法で step 2 及び step 3 分画で相当量のクロムが抽出された場合、あるいはXAFS法で相当量の鉄水酸化物態・腐植物質態・水酸化クロムが検出された場合は、その堆積物試料はかつて六価クロムに暴露されていたことを意味する。