研究テーマ
2、X染色体再活性化ライブイメージング技術を用いた幹細胞研究
将来の再生医療を考えると、iPS細胞のリプログラミング等を含む多能性幹細胞の理解を深める基礎研究は重要です。我々は、H23年から採択されたさきがけ研究「X染色体再活性化 ライブイメージング技術を用いた幹細胞研究」で、幹細胞の未分化性を可視化する技術開発に取り組みました。
近年、ヒトiPS細胞の樹立が報告され、あらゆる種類の細胞、組織に分化できる多能性幹細胞を用いた再生医療への応用に期待が集まっています。これまでの研究から、多能性幹細胞には未分化状態の異なる
細胞種集団があり、種々の細胞に分化する能力(多能性)に違いがあることが分かってきました。未分化状態に近い「ナイーブ状態」と分化が進んだ「プライム状態」です。再生医療への応用を考えるとより多くの種類の
細胞に分化でき、他の個体とのキメラ動物を作ることできるナイーブ状態の細胞の方が、応用範囲が広いと考えられます。ただ、これら異なる状態の細胞を生かしたまま区別する方法が無いことが、幹細胞研究の一つの障害
になっていました。そこで、我々は幹細胞の多能性の指標として利用されている「X染色体再活性化」に注目しました。(幹細胞の多能性とX染色体の再活性化についての詳しい解説はDeuve JLの総説を参照ください。
PubMed Link)。現在、幹細胞の多能性を評価するマーカーとして「X染色体の再活性化」は優れた指標と考えられています(ref.3)。
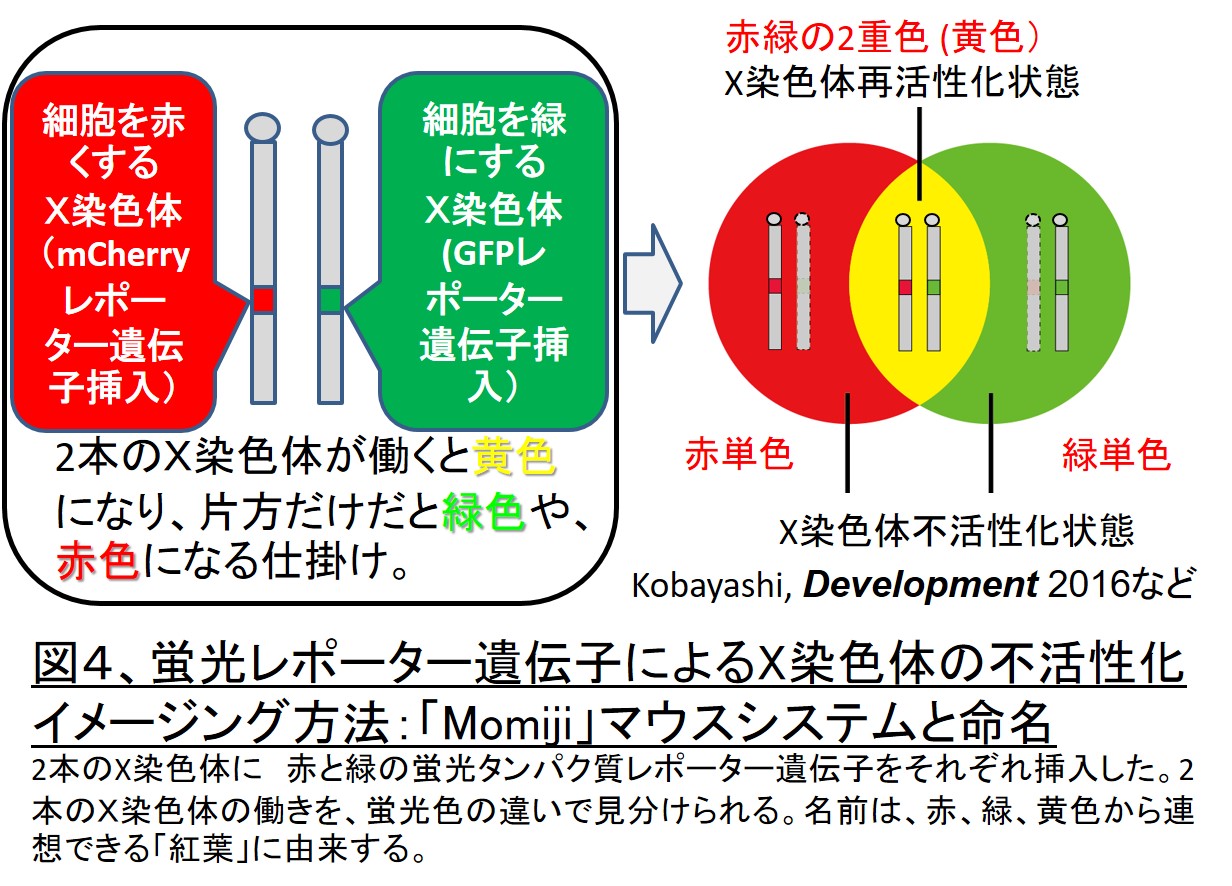
我々のグループではマウスを材料に、X 染色体の活性化状態を生きた細胞で観察するため、2本あるX染色体それぞれの狙った部位に、赤(mCherry)と緑(eGFP)のレポーター遺伝子を挿入した遺伝子組換え動物を開発し、
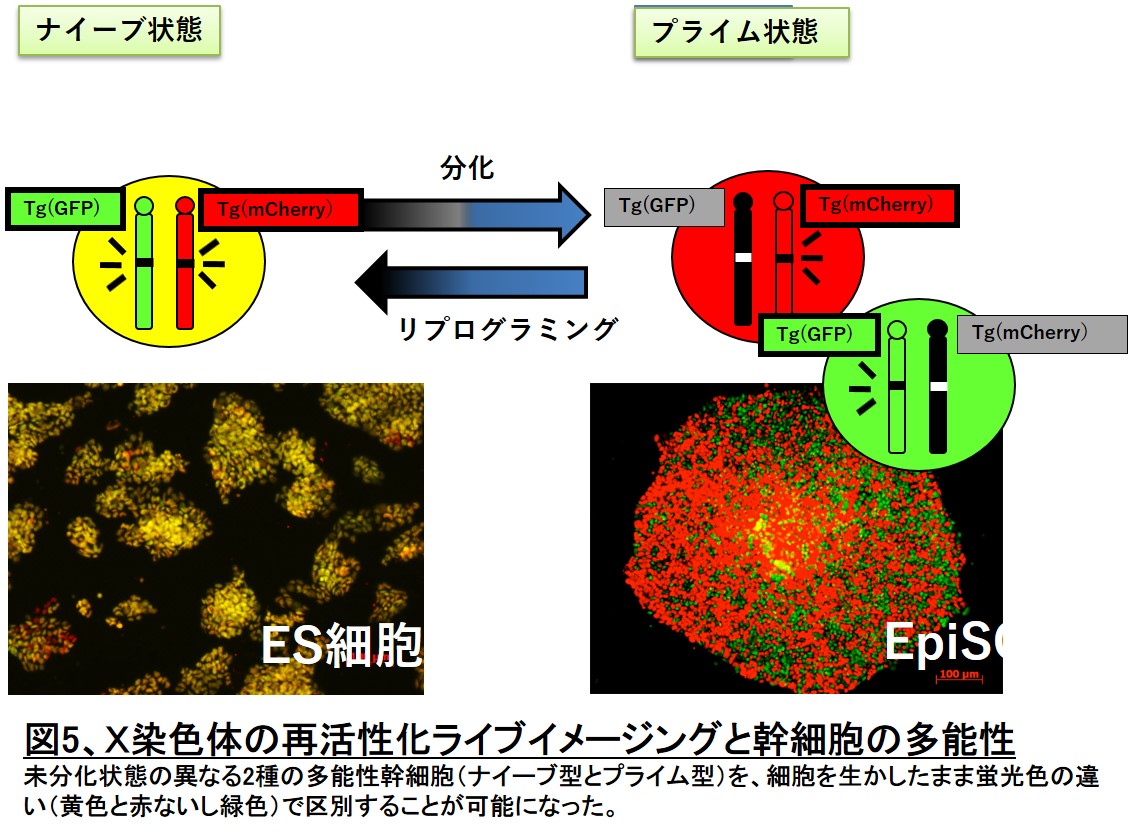
「Momiji」マウスと名前をつけました(図4)。更に、図5に示すようにこの「Momijiマウス」から樹立した多能性幹細胞は、
分化の進んだプライム状態(例:マウスエピブラスト幹細胞:EpiSC)ではX染色体の不活性化を示し赤または緑の単色の蛍光が検出されます。一方、より未分化なナイーブ状態(例、マウス胚性幹細胞:ES細胞)では再活性化が起こり、
赤と緑の蛍光が同時に発現し黄色い蛍光を示します。このように、我々は遺伝子組換えマウスを利用し、X染色体の活性化状態を可視化することにより、初めて細胞を生かしたまま幹細胞の多能性を判別できる技術開発に
成功しました(ref. 2,4&5.)。
現在この技術を利用し、iPS細胞のリプログラミング機構の解明など様々な幹細胞研究課題に取り組んでいます。また、この系の利点は多能性幹細胞それ自体の研究やiPS細胞に関するリプログラミング研究に役立つ
ばかりでなく、発生学におけるエピジェネティクス研究にも有用であることです。マウスの蛍光を見るだけで、発生に従い時事刻々と変化するX染色体の動的なエピジェネティックな変化が一細胞レベルで解析できます。
この系を利用することにより今まで困難であった「発生におけるエピジェネティクスの変化 」を個体を生かしたまま観察することに成功し、報告しました(ref.5 では、着床前胚で、まさにX染色体の不活性化が始まる
瞬間を捉えることに成功しました。movie1 Link)。発生するマウス個体を、一細胞レベルで解析することにより、今まで検出ができなかった
エピジェネティクス制御のバラツキが一個体の中にあることが分かりました。生物とは、一見綺麗に制御されているように見えますが、一つの胚に注目すれば個々の細胞レベルではバラツキがあることが一目瞭然で分かるよう
になりました。現在、”Momijiマウス”を用い発生、組織再生、および発ガン機構など、多能性幹細胞が関わる可能性のある様々な研究課題に取り組んでいます。このように我々は遺伝子組み換え動物を中心として独自の技術、
材料を利用し、幹細胞研究や発生、疾患発症機構におけるエピジェネティクスを対象に研究を進めています。将来これらの研究は、再生医療の臨床応用やヒト疾患の新しい診断方法の確立・治療に繋がることが期待されます。